

Yun He Capital
| 无锡太湖云和科技成果转化创投基金 | 广州南沙云合毅程创业投资基金
| 溧阳云禾添锋智能制造基金 | 湖州云合毅玺创投基金 | 云和县工投产业母基金

云 和 观 点

云和资本合伙人 张波

云和资本高级投资经理 解东洋
长期以来,全球疫苗市场持续扩张,且市场集中度高,GSK、辉瑞等少数几个巨头厂商占据了全球市场的半壁江山。中国一类疫苗市场规模相对较小,主要由国企掌控,二类市场民营企业参与度高,且规模巨大,产品也日趋丰富,优质国产疫苗厂商大有可为。
2020年在新冠肺炎的阴霾下已经过去了一半,全世界都在翘首以盼着出现一种有效的疫苗,这也给全世界的疫苗厂商提供了机遇,同时对疫苗厂商研发能力的提升和政府审批制度的优化也起到了一定的推动作用。《疫苗法》的出台也为疫苗从研发到上市的整个流程提供了法律规范。疫苗市场持续扩大,相关法律日趋完善,同时新疫苗的技术研发也逐渐增大,在此情况下,我国疫苗厂商应该如何抓住机遇,开启国产疫苗新时代?本文即将解答。
【要点提炼】
1、全球疫苗市场持续增长,市场集中度高,大品种独步天下,同类品种迭代效应明显。
全球疫苗市场的集中度非常高。GSK、辉瑞、赛诺菲巴斯德、默沙东四大巨头占据了全球疫苗市场一半以上,且地位难以撼动,TOP5和TOP10疫苗系列占据了全球疫苗市场近30%和39%的份额。疫苗低频消费的特点导致了同类型产品之间的竞争非常残酷,优势品种实现产品迭代,取得市场主流地位。
2、中国市场二类疫苗快速发展,品种日益丰富,优质国产疫苗厂商拥有更大的发展空间。
国内疫苗可分为一类疫苗和二类疫苗,其中二类疫苗占据收入口径市场规模的主要份额,且快速增长。疫苗行业的核心驱动力在于:国内疫苗行业相对分散,未来将趋于集中;国内疫苗企业在研项目逐步进入市场,国产疫苗品种日趋丰富;海外疫苗企业产能有限,产品进口数量不足;部分疫苗具有属地性质,需要因地开发。
3、新冠肺炎下疫苗的发展机遇:CDC的壮大和技术升级
新冠疫情下暴露出疾控的不足和力量的薄弱。疾控的强化有利于疫苗行业的发展:疾控能更多的推动终端疫苗的宣传和接种,有望提升疫苗的渗透率;疾控能根据流行病学和企业合作,推动企业相关的产品研发。疫苗研发有其自身的客观规律,从临床前到最后审评上市仍需要时间,其结果存在不确定性,而通过新冠肺炎疫苗的投入,将有利于相关上市公司进一步增强技术实力,加快新疫苗技术平台的搭建,对公司乃至行业长期的发展起到推动作用。

|一、疫苗行业概述
(一)疫苗概念
疫苗是将病原微生物(如细菌、病毒等)及其代谢产物,经过人工减毒、灭活或利用基因工程等方法制成的用于预防传染病的自动免疫制剂。疫苗保留了病原菌刺激动物体免疫系统的特性。当人体接触到这种不具伤害力的病原菌后,免疫系统便会产生一定的保护物质,如特异性抗体、免疫细胞、活性生理物质等。当人体再次接触到这种病原菌时,人体的免疫系统便会依循其原有的“记忆”,制造更多的保护物质来阻止病原菌的伤害,最终实现对某一种或一类特定疾病的预防。
疫苗分为活疫苗和死疫苗两种。疫苗行业分析指出,常用的活疫苗有卡介苗,脊髓灰质炎疫苗、麻疹疫苗、鼠疫菌苗等。常用的死疫苗有百日咳菌苗、伤寒菌苗、流脑菌苗、霍乱菌苗等。
(二)行业分类
我国市面上的疫苗可以分为第一类疫苗和第二类疫苗。
1. 第一类疫苗
第一类疫苗,是指政府免费向公民提供,公民应当依照政府的规定接种的疫苗,包括国家免疫规划确定的疫苗,省、自治区、直辖市人民政府在执行国家免疫规划时增加的疫苗,以及县级以上人民政府或者其卫生主管部门组织的应急接种或者群体性预防接种所使用的疫苗。
2019年,一类疫苗批签发量为5.78亿人份,国有企业一类疫苗批签发量占国内一类疫苗批签发量的80.36%,是民营企业和外资企业占比总和的4.09倍。市场基本被国企垄断,占比达74%,高于民企与外企的24.3%和1.7%。主要原因为一类疫苗为强制接种疫苗,且由国家医保付费,价格相对较低,利润率较低,因此大多数民企并未涉足该领域。
2. 第二类疫苗
第二类疫苗,是指由公民自费并且自愿接种的其他疫苗。
2019年,二类疫苗累计批签发321.9万支,四价疫苗累计批签发710.7万支,九价疫苗累计批签发239.5万支,HPV疫苗累计1272万支,折合400万人份,保守按2亿潜在可接种人群计算,渗透率仅2%,仍处于供不应求状态。市场中民企占比最高,达67.5%,远高于国企与外企的24.3%和8.1%。二类疫苗毛利高,民企进入该市场的意愿强烈。且二类疫苗对研发的要求更高,创新能力相对较高的民企优势更加明显。
(三)发展历程
自1796年全球首个牛痘用于天花预防的牛痘疫苗出现以来,疫苗产品经历了灭活减毒等常规疫苗时期以及亚单位疫苗、联合疫苗、多糖结合疫苗发展黄金期,目前已进入基因工程疫苗、DNA疫苗等新技术阶段。主要可分为以下四个阶段:

资料来源:《疫苗研究与应用》/云和资本整理
(一)全球疫苗市场
2017年全球疫苗市场规模438亿美元,2013-2017年CAGR为8.7%,在所有治疗领域中位列第四位。伴随着更多的新型疫苗及多价多联疫苗陆续上市,未来全球疫苗市场的增长潜力较大。据预测,到2030年时市场规模可达992亿美元,CAGR为6.5%。

资料来源:长城证券研究所/云和资本整理
全球疫苗市场的集中度非常高。根据灼识咨询提供的最新数据,GSK、辉瑞、赛诺菲巴斯德、默沙东四大巨头占据了全球疫苗市场一半以上份额,且地位难以撼动;TOP5疫苗系列占据了全球疫苗市场近30%的份额,TOP10疫苗系列产品占据全球疫苗市场39%的份额。

资料来源:灼识咨询/云和资本整理
(二)中国疫苗市场
2017年中国人用疫苗市场规模253亿元,2013-2017年CAGR为6.2%。其中:一类疫苗市场37亿元,二类疫苗市场217亿元。据预测,到2030年时规模可达1009亿元,CAGR为11.2%。其中:一类疫苗市场33亿元,二类疫苗市场976亿元。

资料来源:长城证券研究所/云和资本整理
截至到2020年初,国内一类疫苗生产商主要以国企为主,中生集团下六大所和昆明所占据国内超过70%的份额;而二类疫苗市场中,民营企业是主力军,占据约65%的市场份额;外企在整个疫苗市场所占比重不大,目前在二类疫苗市场上的份额约为9%。

资料来源:中检院/云和资本整理
|三、市场格局与竞争分析
(一)产业链总览
目前,中国疫苗市场的供应者大致可分为四类:国有七大所、民企、外企、地方国资委下属企业。
(1)国有七大所包括中生旗下的兰州所、长春所、上海所、北京所、成都所、武汉所,以及由卫健委管辖的昆明所(中国医学科学院医学生物学研究所)。七大所是我国疫苗系统最核心的单位,承载了大量基础疫苗(尤其是一类疫苗)的生产任务。从批签发数据看,七大所批签发占据了市场半壁江山。
(2)民企是疫苗行业的新兴力量,大多成立于1990年-2010年之间。基于对盈利的追求和更灵活的机制,民营企业在创新疫苗研发方面有较好表现。
(3)外企是国内疫苗行业的重要补充,为市场提供多种重要、甚至独家品种。
(4)地方国资委下属企业有国资背景,但缺乏七大所的地位和资源,大多品种较为单一。例如华北制药、金坦生物、长春百克和吉林迈丰、成大生物等。
我国一类疫苗主要由国内七大生物制品研究所生产供应,国有企业占据一类疫苗市场的主导地位。二类疫苗国有企业有先发优势,但是充分竞争后,民营企业占主导,国企和外资占有一定的市场份额。在流通环节,疫苗从经销商→省疾控中心→市疾控中心→县疾控中心→乡镇防疫部门逐级流通。

资料来源:公开资料/云和资本整理
(二)国内产业格局
截止到2020年2月,疫苗行业整体批签发量为10398.2万支,同比提升47%,增幅较1月扩大。现阶段,我国进行批签发机构中检院可独立签发全部疫苗品种;上海所可独立签发指定区域内申请人申报的流感疫苗,批签发机构数量有限。随着未来批签发机构的逐步扩容,行业整体批签发速度预计持续提升。

资料来源:公开资料/云和资本整理
行业整体批签发量前三大类分别是脊髓灰质炎、肝炎、百白破系列三大类疫苗,市场占比分别为21%、19%、18%。肝炎类疫苗批签发量小幅上升2%,市场份额为19%。百白破类疫苗批签发量小幅增加2%,市场份额上升至18%。脊髓灰质炎疫苗批签发量增长13%,市场份额提升至21%,增长份额主要是由口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗来带动的。

资料来源:公开资料/云和资本整理
(三)前沿疫苗平台技术对比
科技发展带来技术革新,国产疫苗行业还有更多发展空间。疫苗技术平台的升级,例如二倍体技术、纳米佐剂疫苗、DNA载体疫苗、重组病毒样颗粒疫苗等。国内疫苗产业的发展落后成熟市场10~20年,未来随着行业的净化和科技的发展,国产疫苗行业还有很大的追赶空间。
|
技术名称 |
描述 |
优点 |
缺点 |
技术难点 |
举例 |
|
重组病毒样颗粒疫苗 |
由病毒的一个或多个结构蛋白在体内或体外自组装而成的空心颗粒 |
组分单一、不含有病毒核酸、良好的安全性、质量可控 |
研究难度大 |
获得合适的放大制备工艺、组装工艺和制剂工艺组合 |
乙肝病毒 VLP 疫苗、人乳头瘤病毒VLP 疫苗、戊肝病毒VLP疫苗等 |
|
DNA 载体疫苗 |
将抗原的基因构建到表达质粒,将此重组质粒转入机体内 |
制备简易、没有感染性、只编码目的蛋白质而不包含其它病毒或细菌蛋白质 |
DNA 进入细胞的效率低、潜在的基因重组可能性、持续表达可能引起的免疫耐受等 |
基因整合技术、避免生殖毒性和免疫耐受等 |
流感病毒疫苗 |
|
纳米佐剂 疫苗 |
纳米粒子既可避免渗入到血管,又可限制其在淋巴管中的传输速度 |
生物靶向作用、延长药物作用时间、缓释药物 |
安全性、局部不良反应 |
不同纳米材料的免疫策略及其理化性质之间的差异 |
伪狂力康 C 株(猪用) |
|
多糖蛋白 结合疫苗 |
多糖抗原与载体蛋白共价结合,是人类最成功的疫苗 |
长久免疫保护 |
在高危人群中免疫原性较低,成本较高,可能产生副反应物 |
多糖与蛋白共价结合并且减少副反应物的产生 |
Hib 多糖结合疫苗、脑膜炎奈瑟球菌多糖结合疫苗、肺炎球菌多糖结合疫苗、百日咳博得特氏菌和白色念珠菌抗菌疫苗 |
|
糖修饰蛋白结合疫苗 |
抗原蛋白与多糖分子共价结合 |
影响蛋白的抗原性和免疫原性,并增强了疫苗的稳定性 |
成本较高,可能产生副反应物 |
恰当选择载体和比例 |
乙肝病毒表面抗原 HBsAg 的疫苗和H5N1 亚型禽流感病毒的HA(血凝素蛋白)抗原等 |
资料来源:《新型疫苗佐剂的研究进展》/云和资本整理
(四)近年来获批/将获批上市的疫苗品种概览
历史上由于疫苗研发周期长、壁垒高、长期没有新品种上市等因素导致国内疫苗产业发展较慢。但自2015年之后,平均每年有接近10个产品获批上市,其中13价肺炎结合疫苗、HPV疫苗、五价轮状病毒疫苗、四价流感疫苗等全球销量排名TOP10的重磅疫苗的me-too产品在2015-2018年期间集中上市,新型重磅疫苗进入爬坡期,将带来行业景气度升级。
|
企业名称 |
药品名称 |
上市/预期上市时间 |
|
荣安生物 |
冻干人用狂犬病疫苗(Vero 细胞) |
2015年 |
|
天坛生物 |
口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) |
|
|
天元生物 |
吸附无细胞百白破联合疫苗 |
|
|
卫信生物 |
吸附无细胞百白破联合疫苗 |
|
|
沃森生物 |
吸附无细胞百白破联合疫苗 |
|
|
延申生物 |
甲型 H1N1 流感病毒裂解疫苗 |
|
|
医科院 |
Sabin 株脊髓灰质炎灭活疫苗 |
|
|
肠道病毒 71 型灭活疫苗(人二倍体细胞) |
||
|
长春所 |
甲型 H1N1 流感病毒裂解疫苗 |
|
|
GSK |
人类乳头瘤病毒吸附疫苗 |
2016年 |
|
辉瑞 |
十三价肺炎球菌结合疫苗 |
|
|
科兴生物 |
肠道病毒 71 型灭活疫苗(Vero 细胞) |
|
|
欧林生物 |
吸附破伤风疫苗 |
|
|
荣盛生物 |
水痘减毒活疫苗 |
|
|
卫尔赛 |
冻干人用狂犬病疫苗(Vero 细胞) |
|
|
雅立峰 |
人用狂犬病疫苗(Vero 细胞) |
|
|
医科院 |
脊髓灰质炎减毒活疫苗糖丸(人二倍体细胞) |
|
|
MSD |
重组人乳头瘤病毒(6 型,11 型,16 型,18 型)疫苗(酵母) |
2017年 |
|
北生研 |
Sabin 株脊髓灰质炎灭活疫苗(Vero 细胞) |
|
|
康希诺 |
重组埃博拉病毒病疫苗 |
|
|
欧林生物 |
b 型流感嗜血杆菌结合疫苗 |
|
|
沃森生物 |
23 价肺炎球菌多糖疫苗 |
|
|
MSD |
口服五价重配轮状病毒减毒活疫苗(Vero 细胞) |
2018年 |
|
九价人乳头瘤病毒疫苗(酿酒酵母) |
||
|
华兰生物 |
A 群C 群脑膜炎球菌多糖疫苗 |
|
|
四价流感病毒裂解疫苗 |
||
|
民海生物 |
23 价肺炎球菌多糖疫苗 |
|
|
卫信生物 |
ACYW135 群脑膜炎球菌多糖疫苗 |
|
|
医科院 |
Ⅰ型+Ⅲ型脊髓灰质炎减毒活疫苗糖丸(人二倍体细胞) |
|
|
口服Ⅰ型Ⅲ型脊髓灰质炎减毒活疫苗(人二倍体细胞) |
||
|
长生生物 |
流感病毒裂解疫苗(四价) |
|
|
康泰生物 |
人用狂犬病疫苗(人二倍体细胞) |
2019年 |
|
沃森生物 |
13 价肺炎球菌多糖结合疫苗 |
|
|
智飞生物 |
预防用微卡(母牛分枝杆菌) |
|
|
康泰生物 |
13 价肺炎球菌结合疫苗 |
2020E |
|
ACYW135 群脑膜炎球菌结合疫苗 |
||
|
脊髓灰质炎 IPV 疫苗 |
||
|
沃森生物 |
重组人乳头瘤病毒双价(16/18 型)疫苗(酵母) |
|
|
智飞生物 |
23 价肺炎球菌多糖疫苗 |
|
|
康希诺生物 |
脑膜炎球菌疫苗 MCV2、MCV4 |
|
|
康泰生物 |
重组肠道病毒 71 型疫苗(汉逊酵母) |
2021E |
|
沃森生物 |
ACYW135 群脑膜炎球菌多糖结合疫苗 |
资料来源:CDE/云和资本整理
|四、《疫苗法》亮点解读
《中华人民共和国疫苗管理法》于2019年6月29日经十三届全国人大常委会第十一次会议表决通过,自2019年12月1日起施行,《疫苗法》共计11章100条,涵盖了从疫苗研制到上市后管理等全流程,是疫苗行业管理的基本法律,对未来疫苗产业的发展将产生深远的影响。
(一)全方位的监管体系
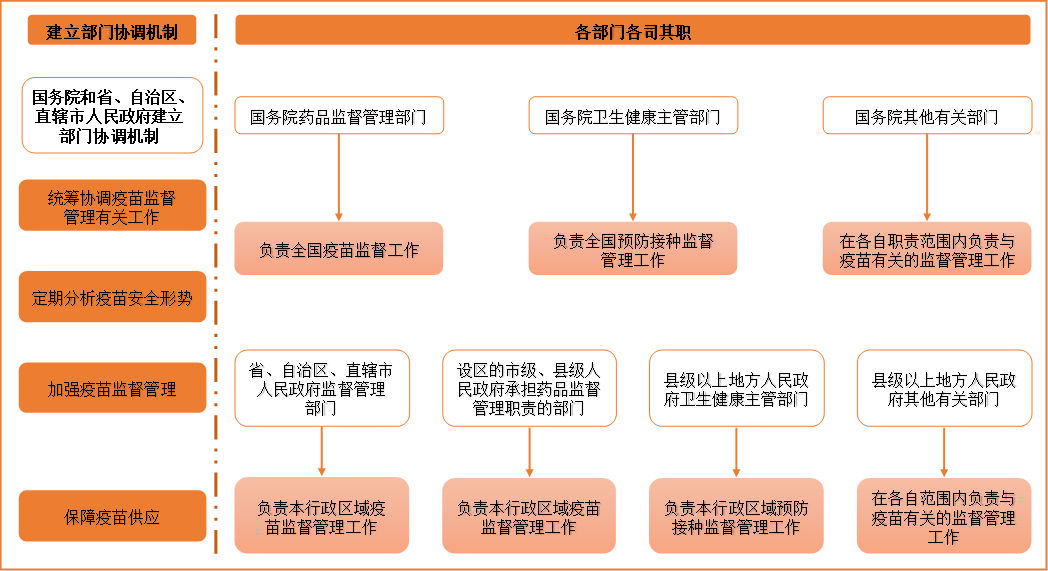
资料来源:《疫苗法》、天凤证券/云和资本整理
(二)实行疫苗全程电子追溯和强制保险制度

资料来源:《疫苗法》、天凤证券/云和资本整理
(三)建立国家免疫规划疫苗动态调整机制
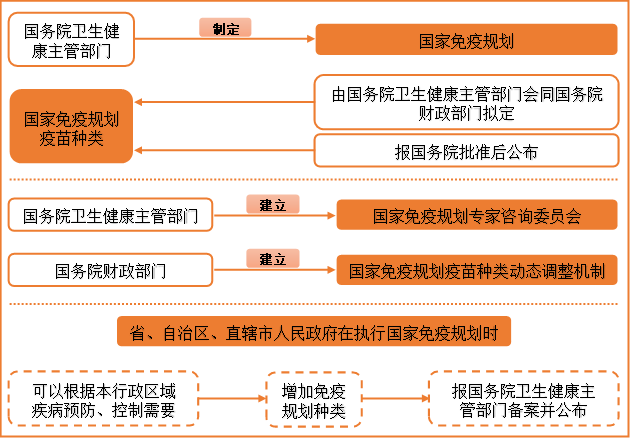
资料来源:《疫苗法》、天凤证券/云和资本整理
(四)支持多联多价等新型疫苗研制

资料来源:《疫苗法》、天凤证券/云和资本整理
(五)坚持疫苗产品的战略性和公益性

资料来源:《疫苗法》、天凤证券/云和资本整理
(六)鼓励出口创造行业增长新空间
1、《疫苗法》第九十八条提出国家鼓励疫苗生产企业按照国际采购要求生产、出口疫苗。出口的疫苗应当符合进口国(地区)的标准或者合同要求。
2、我国已有四款疫苗通过WHO预认证,并被纳入联合国儿童基金会、全球疫苗免疫联盟采购计划,标志着中国疫苗走向世界,随着政策的鼓励,预计后续更多的国产疫苗有望走出国门,造福世界。
通过WHO预认证的四款疫苗
|
疫苗 |
厂家 |
|
乙型脑炎减毒活疫苗 |
成都生物制品研究所 |
|
口服Ⅰ型Ⅲ型脊髓灰质炎疫苗 |
北京北生研生物公司 |
|
流感疫苗 |
华兰生物公司 |
|
甲型肝炎灭活疫苗 |
北京科兴生物公司 |
资料来源:《疫苗法》/公开资料/云和资本整理
|五、展望及建议
(一)未来展望
1、《疫苗法》推动行业三大变化开启中国疫苗产业发展新阶段
长生生物事件推动《疫苗法》出台,《疫苗法》从立法的高度,对疫苗从研发、生产、流通和使用全链条、全周期实施强监管,坚决堵塞监管漏洞,严厉打击违法违规,确保疫苗生产和供应安全,有利于行业规范健康的发展;国家制定疫苗产业发展规划和产业政策,支持疫苗行业的持续发展。《疫苗法》支持行业积极进行创新,推动企业加快技术积累,疫苗行业的创新升级有望加速推进。《疫苗法》支持疫苗产业发展和结构优化,鼓励疫苗生产规模化、集约化。随着疫苗生产质量的不断提升,行业标准进一步提升,不符合要求的企业将逐步退出,行业将加速优胜劣汰,国有企业和大型骨干企业的主导作用将更加凸显,优质企业的优势、稀缺性将进一步体现。
2、我国疫苗产业未来持续扩容,国产疫苗大品种新时代开启
我国疫苗市场将持续扩容,预计到2030年达到1009亿元,年复合增长率达到11.2%,体现出疫苗行业的强劲增长势头。新冠疫情的全民教育,有助于居民健康接种意识的提升,推动行业的持续扩容。高价值二类疫苗迎来良好发展机遇,发展空间大:从未来疫苗发展结构看,二类疫苗将是推动整体市场扩容的主要品类,未来我国疫苗市场高价值大品种疫苗有很大的发展空间。而随着国内企业的持续研发积累,国产大疫苗品种如13价肺炎疫苗、HPV疫苗等逐步上市,开启国产疫苗大品种新时代。
3、新冠肺炎下疫苗的发展机遇:CDC的壮大和技术升级
疾控中心的强化有利于疫苗行业的发展:(1)疾控能更多的推动终端疫苗的宣传和接种,有望提升疫苗的渗透率;(2)疾控能根据流行病学和企业合作,推动企业相关的产品研发。同时习近平主席在朝阳区疾病预防控制中心调研时,也提出:要把全国疾控体系建设作为一项根本性建设来抓,加强各级防控人才,科研力量、立法等建设,推进疾控体系现代化,疾控的整体建设有望迎来新的发展阶段。疫苗研发有其自身的客观规律,从临床前到最后审评上市需要一定时间,结果存在不确定性,而通过新冠肺炎疫苗的投入,将有利于相关上市公司进一步增强技术实力,加快新疫苗技术平台的搭建,对公司乃至行业长期的发展起到推动作用。
(二)潜在风险
1、行业黑天鹅事件:疫苗行业受到国家严格监管,仍不排除企业经营质量管理会有未知问题出现。
2、新品种研发进展低于预期:疫苗产品具有知识密集、技术含量高、风险高、工艺复杂、研发周期长等特点,需要经过临床前研究、临床研究和生产许可三个阶段,并需先后向国家相关部门申请药物临床试验、药品注册批件,接受其严格审核,疫苗产品顺利实现产业化存在一定的不确定性(新产品开发风险)。
3、政策变化风险:疫苗行业属于高度行政监管行业,各个环节都受国家严格监管。《疫苗管理法》的出台,将疫苗行业上升到国家法律层面监管,涵盖了疫苗的研制、生产、流通、预防接种等全过程,对疫苗行业进行全链条、全方位的监管,给疫苗企业提出了更高的要求。
【附录】
附录1:术语表
|
名词 |
解释 |
|
GSK |
葛兰素史克,以研发为基础的药品和保健品公司,年产药品40亿盒,产品遍及全球市场。葛兰素史克由葛兰素威康和史克必成合并而成,于2000年12月成立。 |
|
CDC |
中国疾病预防控制中心,是由政府举办的实施国家级疾病预防控制与公共卫生技术管理和服务的公益事业单位。 |
|
Me-too药物 |
在不侵犯他人专利权情况下,对新出现的突破性新药进行较大的分子结构改造或修饰,寻找作用机制相同或相似,并在治疗应能用上具有某些优点的新药物。 |
|
MSD |
默沙东,位于美国新泽西州肯尼沃斯市的一家公司,除处方药业务,默沙东在中国还包括动物保健业务,近50种兽医产品涉及家畜、家禽和宠物的疾病预防、治疗及控制等多个领域,致力于保护和关怀动物健康以及与其休戚与共的人类健康。 |
|
DTaP-Hib四联疫苗 |
即无细胞百白破b型流感嗜血杆菌联合疫苗,是由百日咳抗原、白喉类毒素、破伤风类毒素和b型流行性感冒嗜血杆菌抗原经过灭活、纯化后联合在一起制成的。可以同时预防多种疾病:百日咳、白喉、破伤风、以及由b型流感嗜血杆菌引起的脑膜炎、肺炎、心包炎、菌血症、会厌炎等疾病。 |
|
HPV疫苗 |
人乳头瘤病毒疫苗。在女性恶性肿瘤中,宫颈癌的发病率仅次于乳腺癌,大多数宫颈癌是由HPV感染所致。2019年12月,国产HPV疫苗获批上市,定价329元/支,适用9-45岁女性。 |
附录2:长生疫苗事件、疫苗法立法重点时间轴说明

资料来源:公开资料/云和资本整理




