

Yun He Capital
| 无锡太湖云和科技成果转化创投基金 | 广州南沙云合毅程创业投资基金
| 溧阳云禾添锋智能制造基金 | 湖州云合毅玺创投基金 | 云和县工投产业母基金

云 和 观 点

云和资本合伙人 张波

云和资本高级投资经理 解东洋
目前,3D传感的主流技术包括:双目视觉、结构光与TOF(Time of Flight)。三种技术各有千秋,双目视觉与结构光主要基于三角定位原理测距。3D TOF技术主要是计算光线飞行的时间,让装置发出脉冲光,并且在发射处接收目标物的反射光,藉由测量时间差算出目标物的距离,从而创建物体或场景的3D深度图。
在行业应用中,消费与汽车将成为3D传感市场的最大增长引擎,其中消费端以手机为主要市场将占据,3D传感的绝大部分份额。
3D传感供应体系中,发射端VCSEL、DOE、WLO、组装以及接收端IR CIS、Filter为全新增量市场,相较于传统彩色摄像头而言创造了新的产业,价值量更大。
【核心要点】
1. 据调查资料显示,预计2022年全球抗肿瘤药物规模将达2000亿美元。截止到2018年,中国抗肿瘤药物规模已达1630亿元,未来5年中国的市场发展空间巨大。
2. 根据国家癌症中心最新发布:《2019年全国癌症报告》指出,肺癌、肝癌、胃癌、结直肠癌以及女性乳腺癌等依然是我国主要的恶性肿瘤。肺癌位居男性发病第1位,而乳腺癌为女性发病首位。城乡恶性肿瘤发病水平逐渐接近。
3. 在抗肿瘤药物发展情况,目前国际上临床常见的抗肿瘤药物约80余种,抗肿瘤靶向药物占据最大市场规模。全球有2000多个肿瘤治疗药品和疫苗正处于不同研发阶段,超过90%为靶向药物,可以说当前全球抗肿瘤药物市场的高速增长是由靶向药物来推动的。

4. 抗肿瘤靶向药物PD-1抑制剂已进入药物商业化阶段。保守估计国内PD-1/L1市场至少500亿元,现已形成“4+4”格局。即4家外企(百时美施贵宝、默沙东、阿斯利康、罗氏)和4家国产第一梯队(君实、信达、恒瑞、百济)。预计进度领先的第一梯队企业将拿下绝大部分市场份额。
5. 抗肿瘤靶向新药研发方面具有高技术、长周期、高成本、高风险以及高回报的特点。在研发流程方面,医药研发外包服务产业链成为了不可或缺的环节,主要合作模式有CRO、CMO和CDMO,该模式覆盖新药研发的各个阶段,包括药物研发、临床前研究、临床试验研究以及商业化生产等,与各类小分子医药企业的研发、采购、生产等整个供应链体系深度对接。
6. 在抗肿瘤靶向药物国内市场发展方面,随着生物制药企业在基础设备,上游研发、中试生产等方面与国外差距的缩小,国内将涌现出大批技术实力较强的企业,靶向药物的市场规模将越来越大,如君实、信达、恒瑞、百济等。
|一、全球抗肿瘤药物市场规模
目前,癌症是全社会需要克服的重大医疗难题之一。据调查数据显示,2012年全球新发病例为1410万,癌症相关死亡人数为820万。2018年癌症新增病例超过170万人次,预计到2030年新发癌症病例数将增加到2360万。受生活环境改变、生存压力增大等各种客观因素的影响,癌症的发病率不断上升。2020年全球癌症发病预计1650.5万人,死亡人数将达1036万人。
2020年全球癌症发病及死亡人数
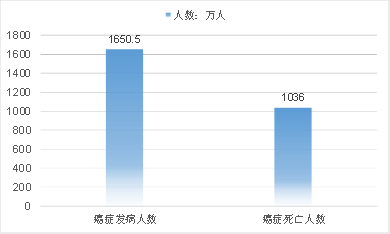
资料来源:智研咨询/云和资本整理
在此背景下,世界抗癌药物市场正在急速增长中,短短5年内全球抗癌药物的市场销售额已翻了一番,并成为最大的细分药品领域,大大超过其他药物的增长。
2013-2022年全球抗肿瘤药物市场规模预测
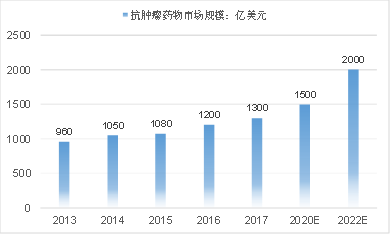
数据来源:公开资料/云和资本整理
2016年,全球在肿瘤治疗药物和维持疗法的市场规模为1200亿美元,是规模最大、增长最快的药物市场。预测这一格局将会持续,到2022年将达到2000亿美元。
|二、中国抗肿瘤药物市场现状
我国肿瘤患病人数居全球之首,发病率和死亡率持续走高,根据2017年国家癌症中心最新数据:全国恶性肿瘤发病率为270.59/10万,死亡率为163.83/10万,预计2030年癌症病发人数将达500万人,死亡人数将达386万人。
2030年中国癌症发病及死亡人数
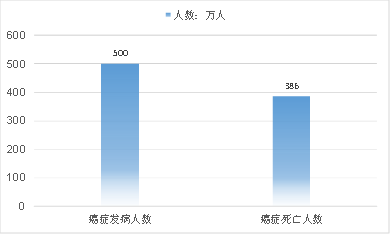
资料来源:公开资料/云和资本整理
2012-2018年,中国抗肿瘤药物市场由620亿元增长至1630亿元,且未来十年的市场空间依然很大。
2012-2018年中国抗肿瘤药物市场规模
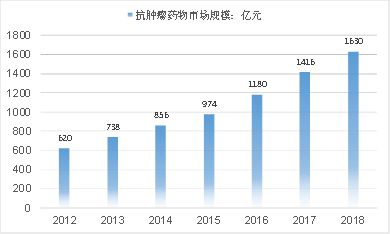
资料来源:智研咨询/云和资本整理
|三、中国主要恶性肿瘤发病情况
2015年恶性肿瘤发病约392.9万人,死亡约233.8万人。平均每天超过1万人被确诊为癌症,每分钟有7.5个人被确诊。与历史数据相比,癌症负担呈持续上升态势。肺癌、胃癌、肝癌、结直肠癌、女性乳腺癌等依然是我国主要的恶性肿瘤。肺癌位居男性发病第1位,而乳腺癌为女性发病首位。
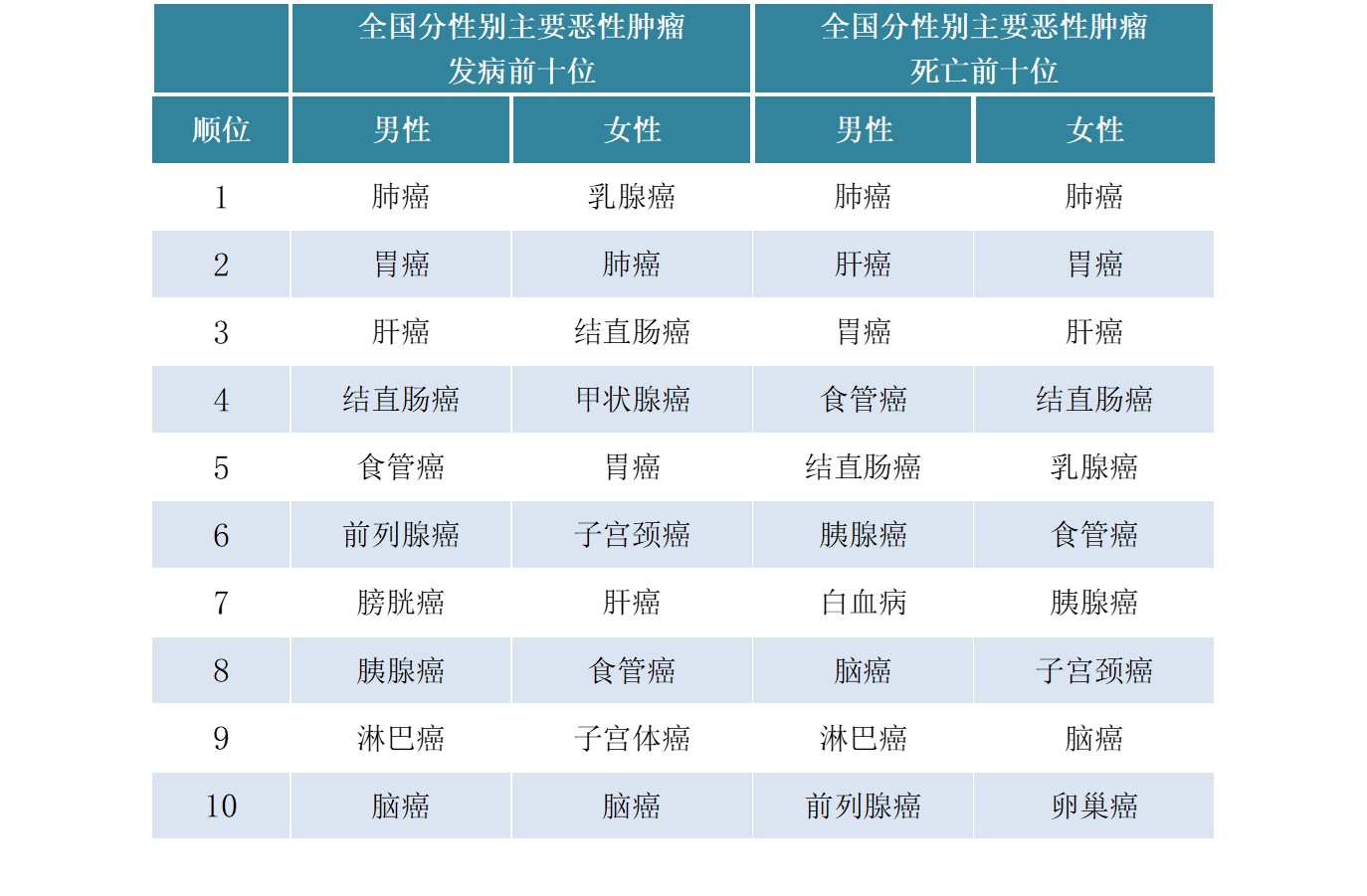
资料来源:国家癌症中心/云和资本整理
城乡恶性肿瘤发病水平逐渐接近,恶性肿瘤负担差异仍然较为明显,表现在城市恶性肿瘤发病率高于农村,而农村恶性肿瘤死亡率高于城市。这可能与城乡癌谱构成差异有关,农村地区主要癌种以上消化系统肿瘤如食管癌、胃癌、肝癌等预后较差的恶性肿瘤为主,城市地区则以结直肠癌和乳腺癌等恶性肿瘤高发。
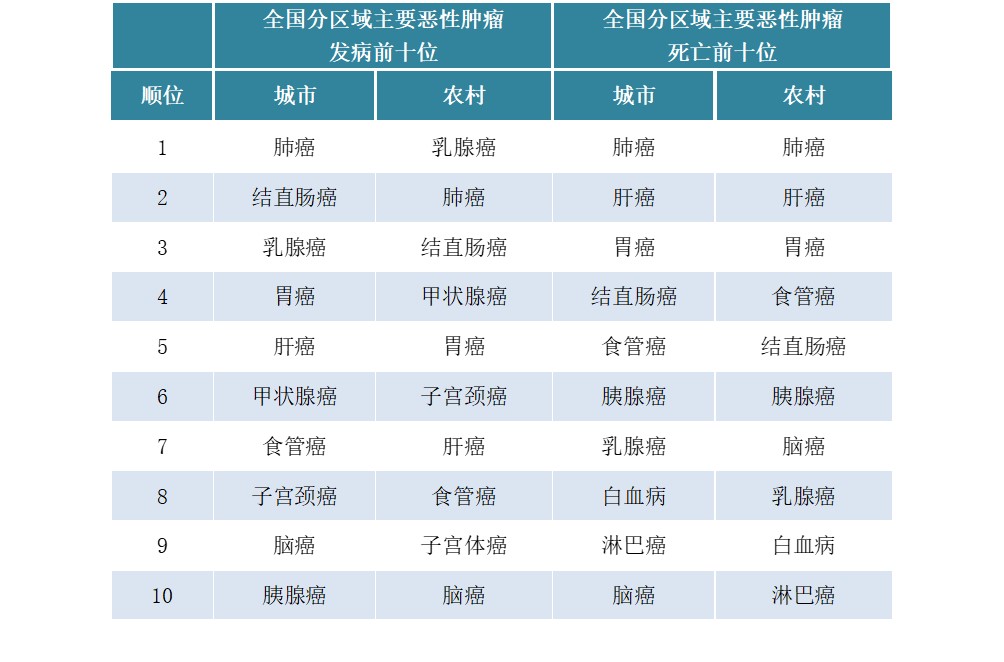
资料来源:国家癌症中心/云和资本整理
总的来说,我国恶性肿瘤负担日益加重,城乡差异较大,地区分布不均衡,癌症防控形势严峻,这迫使我国抗肿瘤药物快速发展。
(一)中国抗肺癌靶向药物简介
肺癌是我国死亡率和发病率均排名第一的恶性肿瘤疾病。根据国家癌症中心2015年的统计数据,我国每年新发肺癌病例约为70万,中国肺癌发病率每年增长高达26.9%。全球常见的肺癌基因突变类型有EGFR、ALK、KRAS等,在不同人种中基因突变类型的分布不尽相同。在中国,非小细胞肺癌患者中最常见的基因突变类型为EGFR基因突变,约占50%。化疗在作用于癌细胞的同时也作用于正常细胞,不可避免带来较大的副作用,增加了患者的痛苦,因此选择针对EGFR的靶向药物是最理想的治疗方案。随着抗癌药物及其相关仿制药的上市,中国抗肺癌药已超过300亿元市场规模。目前已有多个抗肺癌靶向药相继上市:
|
序号 |
药品 |
所属公司 |
|
1 |
阿法替尼(Gilotrif) |
勃林格殷格翰 |
|
2 |
色瑞替尼(Zykadia) |
诺华 |
|
3 |
奥希替尼(Tagrisso) |
阿斯利康 |
|
4 |
阿雷替尼(Alecensa) |
罗氏 |
|
5 |
布吉他滨(Alunbrig) |
武田 |
|
6 |
纳武单抗(Opdivo) |
百时美施贵宝 |
|
7 |
派姆单抗(Keytruda) |
默沙东 |
|
8 |
雷莫芦单抗(Cyramza)、 |
礼来 |
|
9 |
那特珠单抗(Portrazza) |
礼来 |
|
10 |
阿特珠单抗(Tecentriq) |
罗氏 |
资料来源:公开资料/云和资本整理
(二)中国抗肝癌靶向药物简介
在中国,肝癌(HCC)每年发病46.6万人,死亡42.2万人,HCC发病隐匿、侵袭性高,多数患者在确诊时已为中晚期,且常合并有基础性病变,若不经治疗患者整体平均生存期仅为3-6个月。鉴于其恶性程度高,在肿瘤相关病死率中已居第2位。当前,肝癌现有治疗药物如下:
|
序号 |
药物 |
简要说明 |
|
1 |
索拉非尼 |
是全球首个获批上市的口服多靶点激酶抑制剂,由拜耳研发, 2006年获得中国药监局批准进入中国市场,用于治疗不能手术的晚期肝癌患者。 |
|
2 |
仑伐替尼 |
是日本卫材研发的多靶点酪氨酸酶抑制剂,于2018年8月获FDA批准用于一线治疗无法切除的肝细胞癌(HCC),2018年9月中国获批上市。 |
|
3 |
瑞戈非尼 |
拜耳生产的瑞戈非尼为口服多激酶抑制剂,可阻断肿瘤生长和进展过程中参与血管生成、肿瘤形成、转移和肿瘤免疫的多种蛋白激酶。 |
|
4 |
卡博替尼 |
是一种多靶点激酶抑制剂,2019年1月获FDA批准,用于接受过索拉非尼治疗的肝细胞癌患者的二线治疗。 |
|
5 |
雷莫芦单抗 |
是一种单抗药物,通过阻断VEGFR及其下游相关通路促使肿瘤细胞凋亡。2019年5月获FDA批准,用于索拉非尼经治后疾病进展且AFP≥400的肝癌患者二线治疗。 |
|
6 |
PD-1单抗单药 |
2018年11月美国FDA加速批准了帕博利珠单抗用于治疗曾接受索拉非尼治疗的HCC患者肝癌二线治疗(II期)。 |
|
7 |
纳武利尤单抗 |
是一线治疗晚期HCC患者的药物,研究表明,亚洲患者更能从纳武利尤单抗一线治疗中获益。 |
|
8 |
卡瑞丽珠单抗 |
由秦叔逵教授牵头开展,适用于接受过索拉非尼和(或)奥沙利铂为主的系统化疗治疗失败或不可耐受的晚期肝细胞癌患者。 |
资料来源:公开资料/云和资本整理
目前获批的一二线HCC靶向用药数量仍然相对有限,且全部为靶点品种,上述8种药物中前5种为多靶点药物,后3种为单靶点药物。索拉非尼仍为目前肝癌靶向用药领域占比最大的品种,但预计后续将被仑伐替尼超越。
(三)中国抗胃癌靶向药物简介
胃癌是中国每年新发患者数量第三的癌症,仅次于肝癌。在临床治疗中,常根据胃癌患者的TNM分期,选择不同的治疗手段。除胃癌原位癌外,药物化疗伴随其他所有分期的胃癌治疗,氟尿嘧啶类的5-FU或卡培他滨成为胃癌化疗的基础用药,联合其他如铂类药物,还诞生了氟尿嘧啶类复方口服制剂如替吉奥。治疗胃癌的靶向药物开发难度较大,目前仅靶向HER2的曲妥珠单抗和抗血管的雷莫芦单抗进入全身治疗一线或二线及以上用药。全国胃癌化疗药物市场规模在300亿元左右。用药格局上,氟尿嘧啶类作为基础用药其销售额占比最大,为27.58%,其次铂类占比14.9%,紫杉烷类占比13.26%,靶向药物占比12.35%。
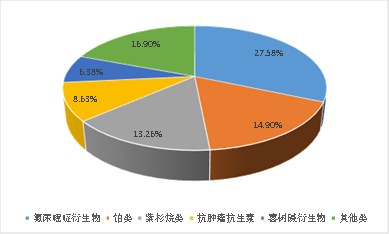
资料来源:公开资料/云和资本整理
目前在晚期胃癌的治疗上,新药和靶点都十分有限,一线系统治疗中仅曲妥珠单抗一个生物药进入指南。PD-1/L1单抗抑制剂在非MSI-H/dMMR晚期胃癌领域的探索较为缓慢,这与胃癌自身生物学和病理学特征有关。但是,从早期的数据来看,仍然有部分患者能够从PD-1抑制剂治疗中获益,因此在临床研究中,需要探索和尝试更多不同的临床方案,一旦取得突破,将会拥有很大的市场竞争力。
|四、抗肿瘤药物发展情况
目前,在药物治疗方面,国际上临床常见的抗肿瘤药物约80余种,按照抗肿瘤药物的传统分类和研究进展,大致可分为以下6类:细胞毒类药物、激素类药物、生物反应调节剂、单/多克隆抗体药物、其他类药物以及辅助药。
临床常见的抗肿瘤药物分类
|
序号 |
分类 |
简要说明 |
|
1 |
细胞毒类药物 |
①作用于DNA化学结构的药物;②影响核酸合成的药物;③作用于核酸转录的药物;④作用于DNA复制的拓扑异构酶Ⅰ抑制剂;⑤作用于有丝分裂M期干扰微管蛋白合成的药物;⑥其他细胞毒药 |
|
2 |
激素类药物 |
①抗雌激素;②芳香化酶抑制剂;③孕激素;④性激素;⑤抗雄激素;†RH-LH激动剂/拮抗剂 |
|
3 |
生物反应调节剂 |
①干扰素;②白细胞介素;③胸腺肽类 |
|
4 |
单/多克隆抗体药物 |
①利妥昔单抗注射液;②注射用曲妥珠单抗;③贝伐珠单抗等 |
|
5 |
其他类药物 |
①细胞分化诱导剂;②细胞凋亡诱导剂;③新生血管生成抑制剂;④表皮生长因子受体抑制剂;⑤基因治疗、细胞分子靶向药物;†瘤苗 |
|
6 |
辅助药 |
①升血药;②止呕药;③镇痛药;④抑制破骨细胞药 |
资料来源:公开资料/云和资本整理
全球60%以上的生物技术成果集中应用于医药工业,用以开发特色新药或对传统医药进行改良,由此引起了医药工业的重大变革,使得生物医药业成为最活跃、进展最快的产业之一。随着分子肿瘤学、分子药理学的发展,肿瘤机理正在逐步阐明。大规模快速筛选、组合化学、基因工程等先进技术的发明和应用,加速了药物开发进程,抗肿瘤药物的研究与开发已进入一个崭新的时代。
在抗肿瘤创新药物的研发方面,当今研究战略有以下特点:
-
以占恶性肿瘤90%以上的实体瘤为主攻对象;
-
从天然产物中寻找活性成分;
-
针对肿瘤发生机制,寻找新的分子作用靶点;
-
大规模快速筛选;
-
新技术的导入和应用:组合化学、结构生物学、计算机辅助设计、基因工程、DNA芯片、药物基因组学等。抗肿瘤药物正从传统单一的细胞毒性药物向在肿瘤发生机理中发挥多环节作用的新型抗肿瘤药物发展。
|五、抗肿瘤靶向药物时代的到来
生物靶向药物是针对肿瘤基因开发的,它能够识别肿瘤细胞上由肿瘤细胞特有基因所决定的特征性位点,通过与之结合(或类似的其他机制),抑制肿瘤细胞内控制细胞生长、增殖的信号传导通路,从而杀灭肿瘤细胞、抑制其增殖。它是随着当代分子生物学、细胞生物学的发展而产生的高科技创新药物,使用靶向药物的治疗方法称为“靶向治疗”。
2017年全球前10大抗肿瘤药全部为靶向抗癌药,其中6种为大分子靶向抗肿瘤药,4种为小分子靶向抗肿瘤药,合计销售541亿美元,占2017年全球抗肿瘤市场份额达47.9%。目前全球有2000多个肿瘤治疗药品和疫苗正处于不同研发阶段,超过90%为靶向药物,可以说当前全球抗肿瘤药物市场的高速增长是由靶向药物来推动的。
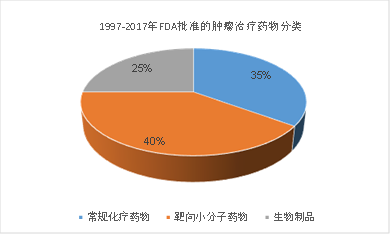
数据来源:公开资料/云和资本整理
鉴于靶向药物特异性高、毒副作用较小,对多种恶性肿瘤具有显著疗效,近十年间已成为抗肿瘤新药的主流,且2016-2017年连续两年FDA批准的新药都是靶向药物。
2012-2017年样本医院抗肿瘤药物与靶向抗肿瘤药物销售额图
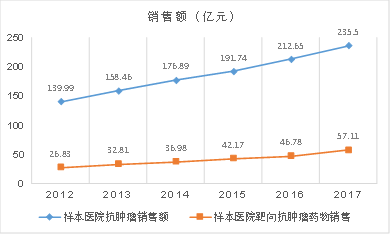
数据来源:公开资料/云和资本整理
2012-2017年靶向抗肿瘤药物与抗肿瘤药物销售额比例图
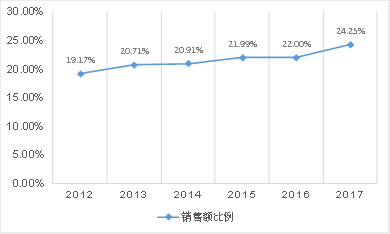
数据来源:公开资料/云和资本整理
随着未来全球老龄化人口上升及新增肿瘤发病例数的增加,抗肿瘤治疗的前景广阔,肿瘤靶向药物治疗效果优异,是未来药物治疗的发展方向。
2019年H1抗肿瘤药在样本医院的市场规模为160亿元。预计2019年全国抗肿瘤市场规模接近1000亿。抗肿瘤药的各个细分类别均持续增长,其中“其他抗肿瘤药”的历年增速最高。该类别主要是靶向抗肿瘤药,占比较高的品种包括曲妥珠单抗、贝伐珠单抗、利妥昔单抗等。可以预见,在未来医院肿瘤用药领域中靶向治疗药物的份额将更大。
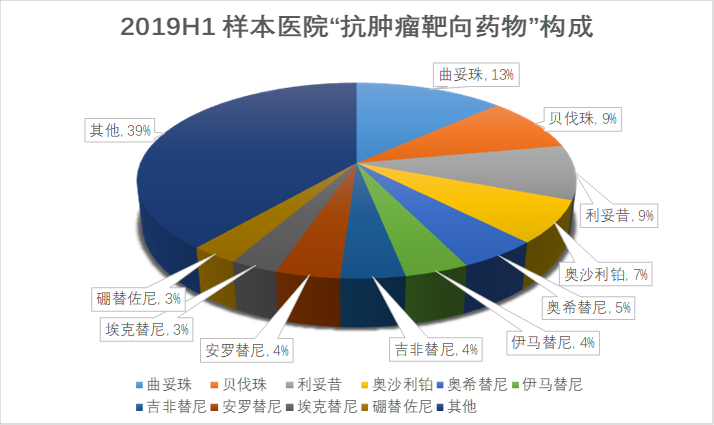
资料来源:智研咨询/云和资本整理
2003年抗肿瘤激素类药物占据了48%的市场份额,但2013年该比例已下降至24%,取而代之的是靶向治疗药物,2013年市场份额为46%,预计单克隆抗体类药物和小分子靶向药物在未来将占据最大的市场份额。
2003-2022年肿瘤治疗药物市场结构及预测
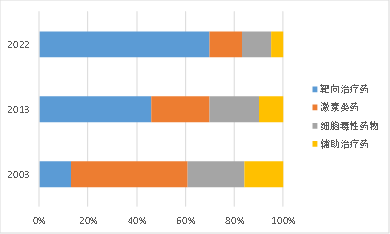
资料来源:公开资料/云和资本整理
靶向药物是针对特定靶点产生作用,每个病人的情况各不相同,可以选用的靶向药物也各有不同,一定程度上实现对肿瘤的个体化治疗。从药品的需求趋势来看,疗效明显、副作用小是未来产品发展的主要需求方向,在这种市场需求驱动下,靶向抗肿瘤药物的研发与临床应用将是抗肿瘤药物行业未来主要发展方向。
|六、抗肿瘤靶向药物明星代表PD-1抑制剂
PD-1(programmed cell death protein 1),也就是程序性死亡受体-1,是一种重要的免疫抑制分子。以PD-1为靶点的免疫调节对抗肿瘤、抗感染、抗自身免疫性疾病及器官移植存活等均有重要的意义。
PD-1/PD-L1 Inhibitors的作用机制
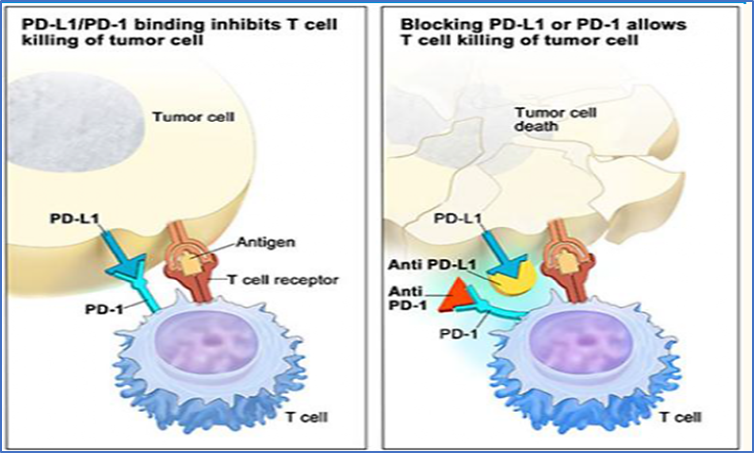
资料来源:公开资料/云和资本整理
当淋巴细胞上的PD-1与其相应的受体PD-L1结合后,会抑制淋巴细胞活化,这是免疫系统中一种正常的自稳机制,因为过度的T细胞激活会引起自身免疫病。当肿瘤细胞的PD-L1与淋巴细胞上的PD-1大量结合后,会抑制T细胞功能,使得肿瘤逃逸机体内的免疫清除。PD-1单克隆抗体的作用机制即为阻断体内PD-1与配体PD-L1之间的结合,使T细胞发挥正常功能,进而利用自身免疫将肿瘤细胞消灭。
(一)全球PD-1/PD-L1抗体市场规模
根据智研咨询发布的数据显示:2018年全球PD-1/PD-L1单抗销售额162.6亿美元,同比增长66%,未来有望成为全球销售额最大的药品品类。
2014-2018年全球PD-1/PD-L1抗体市场规模走势图
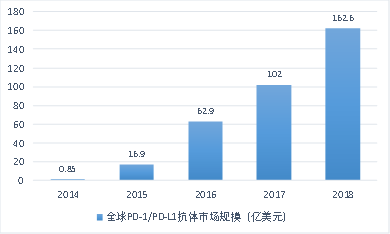
资料来源:智研咨询/云和资本整理
全球首个PD-1/PD-L1抗体Opdivo于2014年7月在日本上市。美国市场上,Keytruda于2014年9月首个上市。2018年,Opdivo和Keytruda销售额分别达到75.7亿和71.7亿美元,同比增长32%和83%,都位居全球销售额前10大药品之列。2019年上半年,Keytruda实现收入49亿美元,已经超过Opdivo的40亿美元。
(二)中国PD-1/PD-L1抗体发展现状
国内PD-1/PD-L1单抗市场已经从药物研发阶段进入药物商业化阶段。2018年6月15日,纳武利尤单抗(BMS)获得NMPA批准上市,成为国内首个获批上市的PD-1单抗。在随后短短的1年时间内,NMPA先后批准上市了5款PD-1单抗,其中2款为进口(纳武利尤单抗,BMS;帕博利珠单抗,默沙东),3款为国产(拓益,君实生物;达伯舒,信达生物;艾立妥,恒瑞医药)。截止目前,另外3款PD-1/PD-L1单抗(替雷利珠单抗,百济神州;度伐鲁单抗,阿斯利康;阿替利珠单抗,罗氏)也已经向NMPA提交了上市申请。
国内PD-1/PD-L1单抗的新药申报情况
|
公司 |
通用名 |
靶点 |
CDE受理号 |
状态 |
适应症 |
|
BMS |
纳武利尤单抗 |
PD-1 |
JXSS1700015/16 |
已批准 |
非EGFR/ALK突变的NSCLC(2线) |
|
纳武利尤单抗 |
PD-1 |
JXSS900001/02 |
在审评审批 |
||
|
默沙东 |
帕博利珠单抗 |
PD-1 |
JXSS1800002 |
已批准 |
黑色素瘤(2线) |
|
帕博利珠单抗 |
PD-1 |
JXSS1800025 |
在审评审批 |
鳞状NSCLC(1线联合卡铂和紫杉醇) |
|
|
帕博利珠单抗 |
PD-1 |
JXSS1800048 |
在审评审批 |
PD-L1阳性的NSCLC(1线) |
|
|
帕博利珠单抗 |
PD-1 |
JXSS1800018 |
已批准 |
非EGFR/ALK突变的非鳞状NSCLC(1线联合培美曲塞和顺铂/卡铂) |
|
|
君实生物 |
特瑞普利单抗 |
PD-1 |
CXSS1800006 |
已批准 |
黑色素瘤(2线) |
|
信达生物 |
信迪利单抗 |
PD-1 |
CXSS1800008 |
已批准 |
复发/难治性经典型霍奇金淋巴瘤(3线) |
|
恒瑞医药 |
卡瑞利珠单抗 |
PD-1 |
CXSS1800009 |
已批准 |
复发/难治性经典型霍奇金淋巴瘤(3线) |
|
卡瑞利珠单抗 |
PD-1 |
CXSS1900023 |
在审评审批 |
批肝细胞癌(2线) |
|
|
百济神州 |
替雷利珠单抗 |
PD-1 |
CXSS1800019 |
在审评审批 |
复发/难治性经典型霍奇金淋巴瘤 |
|
替雷利珠单抗 |
PD-1 |
CXSS1900025 |
在审评审批 |
尿路上皮癌(2线) |
|
|
阿斯利康 |
度伐鲁单抗 |
PD-L1 |
JXSS1800040/41 |
在审评审批 |
Ⅲ期NSCLC |
|
罗氏 |
阿替利珠单抗 |
PD-L1 |
JXSS1900004 |
在审评审批 |
NSCLC(2线) |
资料来源:智研咨询/云和资本整理
国内已上市及正在进行中后期临床试验的PD-1/PD-L1单抗药物多达有20个,包括13个PD-1单抗和7个PD-L1单抗。BMS、默沙东、君实生物、信达生物和恒瑞医药的PD-1单抗从2018年6月开始已陆续获批上市,同时百济神州的PD-1单抗以及罗氏和阿斯利康的PD-L1单抗正在进行上市申请。
2019年天风证券生物医药行业报告指出:保守估计国内PD -1/L1市场至少500亿元,现已形成“4+4”格局。尽管国内布局的企业数量众多,但实质上该领域基本形成“4+4 ”格局,即4家外企(百时美施贵宝、默沙东、阿斯利康、罗氏)和4家国产第一梯队(君实、信达、恒瑞、百济)。预计进度领先的第一梯队企业将拿下绝大部分市场份额。
国内PD-1/PD-L1单抗市场竞争格局
|
序号 |
药品 |
靶点 |
公司 |
国内研发进展 |
国内临床获批日期 |
|
1 |
Opdivo |
PD- |
1BMS |
2017/11/2上市申请 2018/6/15获批 |
2015/11/11(临床公示日期) |
|
2 |
Keytruda |
PD-1 |
默沙东 |
2018/2/11上市申请 2018/7/20获批 |
2016/6/6(临床公示日期 |
|
3 |
JS001 |
PD-1 |
君实生物 |
2018/3/9上市申请2018/12/17获批 |
2016/1/4 |
|
4 |
IBI308 |
PD-1 |
信达生物 |
2018/4/19上市申请 2018/12/24获批 |
2016/9/4 |
|
5 |
SHR1210 |
PD-1 |
恒瑞医药 |
2018/4/23上市申请 2019/5/29获批 |
2016/2/4 |
|
6 |
BGB-A317 |
PD-1 |
百济神州 |
2018/9/6上市申请 |
2016/9/3 |
|
7 |
Imfinzi |
PD-L1 |
阿斯利康 |
2018/12/26上市申请 |
2017/1/19(临床公示日期) |
|
8 |
Tecentriq |
PD-L1 |
罗氏 |
2019/2/25上市申请 |
2016/7/6(临床公示日期) |
|
9 |
杰诺单抗 |
PD-1 |
嘉和生物 |
Ⅱ期临床 |
2016/12/8 |
|
10 |
KN035 |
PD-L1 |
思路迪/康宁杰瑞 |
Ⅱ期临床 |
2016/12/28 |
|
11 |
GLS-010 |
PD-1 |
药明康德/誉衡药业 |
Ⅱ期临床 |
2017/3/15 |
|
12 |
CS1001 |
PD-L1 |
基石药业/拓石药业 |
Ⅲ期临床 |
2017/7/17 |
|
13 |
SHR-1316 |
PD-L1 |
恒瑞医药 |
Ⅲ期临床 |
2017/9/14 |
|
14 |
BAT1306 |
PD-1 |
百奥泰生物 |
Ⅱ期临床 |
2017/9/14 |
|
15 |
AK105 |
PD-1 |
康方生物 |
Ⅲ期临床 |
2017/9/14 |
|
16 |
KL-A167 |
PD-L1 |
科伦药业 |
Ⅱ期临床 |
2017/9/27 |
|
17 |
LZM009 |
PD-1 |
丽珠医药 |
Ⅰ期临床 |
2017/10/26 |
|
18 |
TQB2450 |
PD-L1 |
正大天晴 |
Ⅱ期临床 |
2017/11/1 |
|
19 |
HLX10 |
PD-1 |
复宏汉霖 |
Ⅱ期临床 |
2018/3/20 |
|
20 |
SSI-361 |
PD-1 |
安科生物 |
Ⅰ期临床 |
2019/3/18 |
资料来源:智研咨询/云和资本整理
(三)联合用药成为临床试验的主要布局方向
从海外市场来看,罗氏等大药企利用旗下单抗药物优势,专注联合用药疗法的开发,斩获了4种肿瘤的一线治疗方案,使其PD-L1单抗的市场份额逐年增加。而在国内,头部企业凭借旗下产品线较广的优势,获得更多的领先,比如恒瑞医药的PD-1单抗已经联合阿帕替尼进行了针对多种肿瘤的临床试验,临床疗效远高于单药治疗。
从国内PD-1/PD-L1单抗的头部企业主要中后期临床进展来看,联合用药的布局已经占据50%以上,已经成为各大药企研发的重中之重。由于PD-1/PD-L1单抗的联合用药临床疗效非常好,一方面可以增加临床试验的成功率,另一方面可以利用NMPA的优先审评政策,加快获批速度,抢占市场。而对于目前PD-1/PD-L1单抗研发落后的企业,联合靶向小分子药物和单抗药物,凭借其良好的疗效,在尚未获批的适应症上获得有条件申请上市将是一个弯道超车的好机会。
国内头部企业PD-1/PD-L1单抗联合用药在主要后期临床试验中的占比
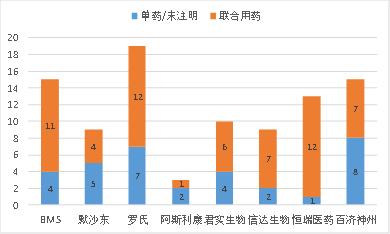
资料来源:CDE、智研咨询/云和资本整理
|七、抗肿瘤靶向新药研发流程分析
(一)研发流程概述
药物从最初的实验室研究到最终摆放到药柜销售平均需要花费12年的时间。总的来说新药研发分为两个阶段:研究和开发。这两个阶段是相继发生且互相联系的。区分两个阶段的标志是候选药物的确定,即在确定候选药物之前为研究阶段,确定之后的工作为开发阶段。具体过程和相应阶段所需时间如下图所示:
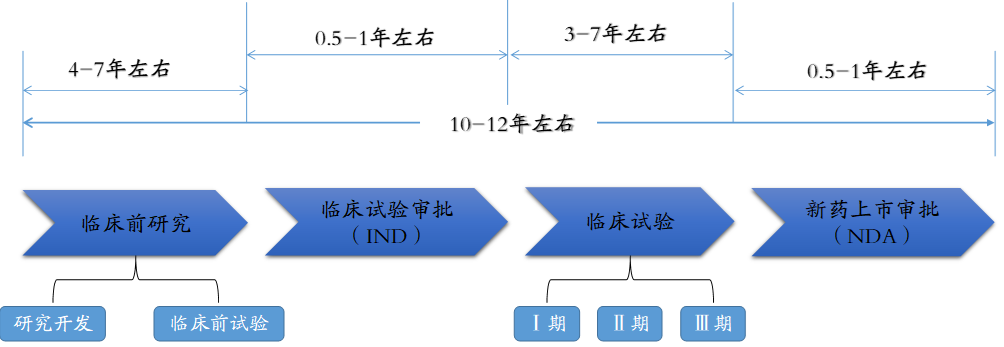
资料来源:云和资本整理
新药的研发过程有着很明显的特点:
1、高技术:这主要表现在其高知识层次的人才和高新的技术手段。生物制药是一种知识密集、技术含量高、多学科高度综合互相渗透的新兴产业。
2、长周期:生物药品从开始研制到最终转化为产品要经过很多环节:实验室研究阶段、中试生产阶段、临床试验阶段(I、II、III期)、规模化生产阶段、市场商品化阶段以及监督每个环节的严格复杂的药政审批程序,而且产品培养和市场开发较难;所以开发一种新药周期较长,一般需要10-12年时间左右。
3、高成本:生物制药是一个投入相当大的产业,目前国外平均开发一个新药的成本为25亿美元。其中每个上市药物的平均研发开支为14亿美元,由于临床试验失败、研发时间长导致的研发费用损失为11亿美元。
4、高风险:新药研发过程中技术上也会有高失败率,上千种新化学单体中可能只有少数几个是可以进入后期候选物质中的。除了技术上,还要面临资金、政策、市场上的各种风险。
(1)新品种开发失败风险是创新药开发需面对的首个重大风险。除研发本身的长周期、高投入、高失败风险以外,更为不利的是,创新药研发各阶段成功率的差异与适应症以及企业在相关方向上的先期积累是否深厚更为紧密。这意味着大公司在介入以往没有相关积累的领域时,很难提升研发成功率。
(2)市场运作风险是创新药开发成功后即需面对的风险。拥有一个好药和靠它来赚钱之间的差距就是市场运作的力量。在一个竞争变得越发激烈的市场中,创新药的成功除了必须有良好的效果,市场运作也至关重要。市场运作失利可以让好药失败,市场运作成功也可以让效果并非显著优于先行者的药物取得意外成功。
(3)竞争风险。市场大、药品效果优异绝对不等于药品前景一定好。创新药在一个足够大的市场中想成为爆款,需要既拥有更好的疗效,也拥有专利保护等壁垒以确保良好的竞争格局,二者缺一不可。
5、高回报:生物药物的利润回报率很高。一种新生物药品一般上市后2-3年即可收回所有投资,尤其是拥有新产品、专利产品的企业,一旦开发成功便会形成技术垄断优势,利润回报能高达10倍以上。
(二)医药研发外包服务产业链
随全球药品市场竞争日益激烈,制药产业链中的分工日趋显著,医药企业呈现出将自身研发与生产业务委托给其他专业化公司开展的大趋势。医药研发生产服务领域覆盖新药研发的各个阶段,包括药物研发、临床前研究、临床试验研究、商业化生产等,与各类小分子医药企业的研发、采购、生产等整个供应链体系深度对接,使附加值较高的技术输出取代单纯的产能输出,为客户提供创新性的工艺研发及规模化生产服务。
国内医药外包服务产业链图谱
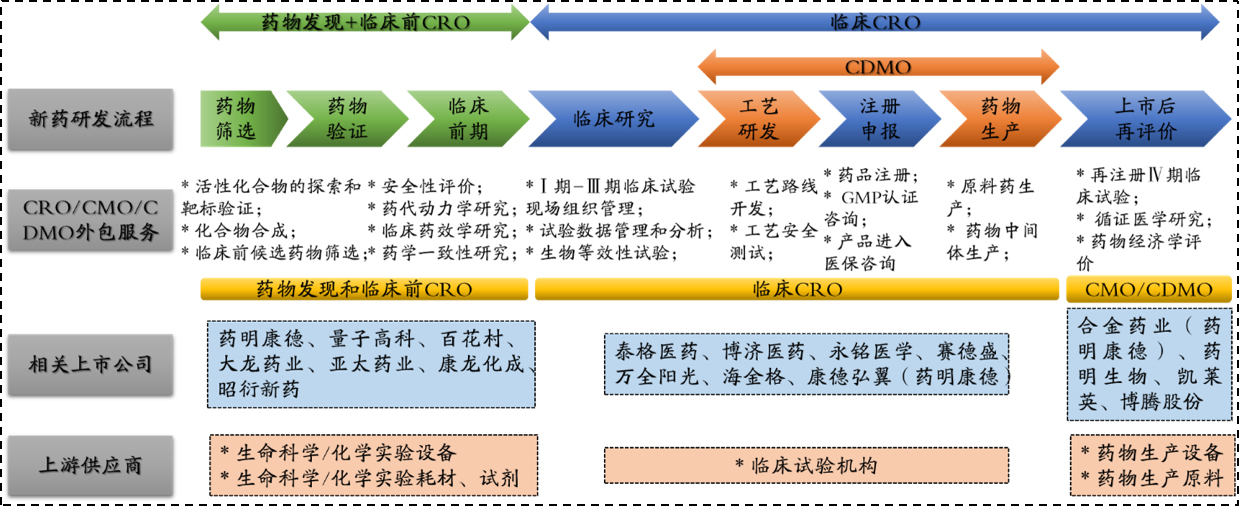
资料来源:云和资本整理
由此衍生出医药研发外包服务产业链,主要包括CRO、CMO和CDMO三种模式。医药研发外包(CRO)是一个新兴的,具有专属性的科研服务性行业,其承接的是生物医药创新型药物研究过程中某一部分专业性较强的,且又能与研究整体融合互补的工作。医药生产外包服务企业(医药CMO)是以合同定制形式为制药企业提供临床用药、中间体制造、原料药生产、制剂生产以及包装等专业服务的企业。从产业链来看,合同生产研发业务(CDMO)处于药物研发至商业化销售的中间关键环节,其上游为临床前研发CRO环节,下游为药品上市后持续的CMO生产环节。由于创新药领域不断发展、研发成本和风险居高不下,越来越多的下游医药制造企业会选择CMO/CDMO服务,以便为医药企业节约成本、控制风险并提升研发效率。
【总结】
综合以上信息,未来随着大量资金和人才的涌入,国内生物制药领域将进入快速发展时期,尤其是对抗肿瘤靶向单抗药物的研发已成为焦点之一。随着资本机构的介入以及当前新药研发模式的变化,新药研发速度将大大提升。2018年动脉新医药指出:抗体药物/靶向药、罕见病、基因治疗成2018年资本热投三大领域,且靶向药/抗体药物投资坐稳头把交椅。由此看出,VC/PE投资机构也愈发重视具有真正创新能力的药企。随着国产生物药品的陆续上市,国内生物制药企业在基础设备、上游研发、中试生产等方面与国外差距缩小,涌现出大批技术实力较强的企业,如君实、信达、恒瑞、百济等,靶向药物的市场规模将越来越大。政策红利方面,国家谈判品种不纳入药占比考核,扫除放量障碍,有利于抗肿瘤靶向药物的市场增长。靶向药物不仅是当前抗肿瘤药物极其重要的一部分,在未来也将成为整个医药行业中最具潜力,增长最强劲的领域。
附录:专业术语
|
PD-1 |
指 |
programmed cell death protein 1,也就是程序性死亡受体-1,是一种重要的免疫抑制分子。 |
|
PD-L1 |
指 |
肿瘤细胞膜上的一种小分子蛋白,为PD-1的受体。 |
|
T 细胞 |
指 |
胸腺依赖性淋巴细胞,是淋巴细胞的主要组分,它具有多种生物学功能。 |
|
Opdivo |
指 |
中国国内首个获批上市的PD-1抗癌药,中文名"欧狄沃",简称O药。 |
|
Keytruda |
指 |
阻断PD-1的细胞通路的第一个被批准的药物,它限制机体免疫系统攻击黑色素瘤细胞的。 |
|
BMS |
指 |
百时美施贵宝公司,是一家以科研为基础的全球性的从事医药保健及个人护理产品的多元化企业,其主要业务涵盖医药产品、日用消费品、营养品及医疗器械。 |
|
NMPA |
指 |
国家药品监督管理局 |
|
TNM |
指 |
肿瘤学中对肿瘤的一种分期形式(T是原发灶,N是淋巴结,M是远处转移 )。 |
|
MSI-H/dMMR |
指 |
微卫星高度不稳定/错配修复缺陷 |
|
KLT-1101 |
指 |
重组人白介素-12 |
|
NK细胞 |
指 |
自然杀伤细胞,是机体重要的免疫细胞,不仅与抗肿瘤、抗病毒感染和免疫调节有关,而且在某些情况下参与超敏反应和自身免疫性疾病的发生。 |
|
B细胞 |
指 |
B淋巴细胞,在抗原刺激下可分化为浆细胞,浆细胞可合成和分泌抗体(免疫球蛋白),主要执行机体的体液免疫。 |
|
CD8+ T细胞 |
指 |
群集分化8,是作为协同受体的T细胞受体(TCR)的跨膜糖蛋白。 |
|
CAR-T |
指 |
嵌合抗原受体T细胞免疫疗法。 |
|
CDE |
指 |
药物审批中心 |
|
CRO |
指 |
医药研发外包 |
|
CMO |
指 |
医药生产外包 |
|
CDMO |
指 |
定制研发生产 |




